这篇题为《Hyperhomocysteinemia-induced VCID results in visual deficits,reduced neuroinflammation and vascular alterations in the retina》的研究文章,发表于2025年的《Journal of Neuroinflammation》,主要研究了高同型半胱氨酸血症(HHcy)诱导的血管性认知障碍与痴呆(VCID)对视网膜结构、功能及炎症反应的影响,探讨视网膜作为VCID生物标志物的潜力。研究由美国印第安纳大学医学院Stark神经科学研究所与肯塔基大学Sanders Brown老龄化研究中心合作完成,通讯作者为Erica M.Weekman博士(印第安纳大学医学院)。

一、研究背景与目的
背景:
老龄化社会中,痴呆的发病率不断上升。
阿尔茨海默病(AD)和**血管性认知障碍(VCID)**是最常见的两种痴呆类型。
目前诊断手段(PET、MRI)成本高、特异性有限。
视网膜作为中枢神经系统的延伸,因其易观察、结构相似,成为潜在的生物标志物来源。
已有研究发现AD对视网膜有影响,但VCID(尤其是脑小血管病,cSVD)对视网膜的影响尚不明确。
目的:
利用HHcy诱导的cSVD小鼠模型,研究其对视觉功能、视网膜细胞结构、炎症与血管相关基因表达的影响。
探讨视网膜是否可作为VCID的生物标志物。
二、研究方法
1.动物模型与处理
使用C57Bl6/SJL小鼠,6月龄,分为两组:
HHcy组(N=18):喂食缺乏B6、B12、叶酸但富含蛋氨酸的饮食(TD.130867)。
对照组(N=20):正常饮食(TD.01636)。
持续14周后,进行行为学与组织学分析。
2.行为学测试:Visual-Stimuli 4-arm Maze(ViS4M)
用于评估小鼠对不同颜色(红、绿、蓝、白)光线的视觉反应。
测试不同光照强度下的视杆细胞(rods)与视锥细胞(cones)功能。
还设置了对比敏感度测试(Contrast condition)。
3.组织学与分子生物学分析
免疫荧光染色:标记视网膜中的血管(Ly6c)、小胶质细胞(IBA-1)与星形胶质细胞(GFAP)。
NanoString基因表达分析:检测神经炎症与心血管相关基因表达变化。
qPCR验证:部分基因表达结果进行验证。
三、主要研究结果
1.视觉功能受损
HHcy小鼠在蓝光和白光刺激下的反应显著下降,进入蓝光/白光臂的次数减少,停留时间缩短。
在Red High和Equal条件下最为明显。
交替行为(alternations)减少,提示空间记忆受损。
对比敏感度未受影响,说明主要影响的是视锥细胞功能,而非视杆细胞。
2.视网膜细胞结构变化
小胶质细胞与星形胶质细胞的数量与体积无显著变化。
血管数量略有减少,尤其在内层视网膜。
血管总体积减少,但单个血管体积未变。
小胶质细胞与血管的接触显著减少,尤其在外层视网膜。
星形胶质细胞与血管的接触无显著变化。
3.基因表达变化
神经炎症与心血管相关基因多数下调:
包括Lgals3、Ccl2、Csf1、Tlr2、Il17a、Nfkbia等。
这些基因与小胶质细胞激活、炎症反应、血管功能密切相关。
视杆与视锥细胞相关基因表达上调(如Pde6g、Gngt2、Pde6c等),可能是代偿性反应。
四、讨论与意义
1.HHcy对视网膜的影响
HHcy诱导的VCID可导致视觉功能下降,尤其是蓝光感知能力。
视网膜血管结构轻微受损,但小胶质细胞与血管的相互作用显著下降,提示神经血管耦合受损。
炎症反应下调,与其他研究(如AD模型)不同,提示VCID与AD在视网膜病理机制上存在差异。
2.与AD模型的比较
AD模型中常见视杆与视锥功能下降、对比敏感度受损。
本研究中HHcy模型主要影响视锥细胞,对比敏感度未受影响。
说明不同病因导致的痴呆在视网膜表现不同,未来开发视网膜生物标志物时需区分病因。
3.研究局限性
未进行蛋白水平验证(如ELISA、免疫组化)。
小鼠模型仅模拟单一病因(HHcy),而人类患者多为多因素混合性痴呆。
视网膜组织有限,未能深入分析视杆/视锥细胞结构变化。
五、结论与展望
HHcy诱导的VCID可导致视网膜功能与结构的特定变化,包括视觉反应下降、血管改变、小胶质细胞与血管互动减少、炎症基因下调。
视网膜有潜力成为VCID的生物标志物,但需进一步研究其机制与在人类中的适用性。
未来研究应:
验证蛋白水平变化;
比较AD与VCID共病模型;
探索人类视网膜与VCID的关联。
图1:高同型半胱氨酸血症(HHcy)损害视觉与认知功能

图注翻译与解释:
A:ViS4M测试中“红光高亮(Red High)”和“光照均等(Equal)”条件下的光照强度(lux)值。
显示不同颜色臂(红、蓝、白、绿)在这两种测试条件下的光照强度,用于控制视觉刺激强度。
B:在Red High和Equal条件下,小鼠进入各个颜色臂的次数百分比。
HHcy小鼠进入蓝光和绿光臂的次数明显减少,提示对这些颜色光的反应减弱。
C:在Red High和Equal条件下,小鼠在各个颜色臂中停留的时间。
HHcy小鼠在蓝光臂中停留时间显著减少,进一步说明其对蓝光敏感性下降。
D:在Red High和Equal条件下,小鼠在迷宫中进行的交替行为(alternations)百分比。
HHcy小鼠进行3臂交替(3-arm alternations)减少,2臂交替增加,提示空间记忆或认知灵活性下降。
E:路径示意图,展示Path 1、Path 2、Path 3三种典型路径。
用于分析小鼠在迷宫中的探索策略。
F:在Red High和Equal条件下,小鼠选择不同路径的比例。
HHcy小鼠更倾向于选择Path 3(即不穿越中心,只在一侧活动),提示其行为模式更刻板。
G:在Red High和Equal条件下,小鼠在不同颜色臂之间的双向转换(bidirectional transitions)次数。
HHcy小鼠在蓝↔绿、蓝↔白之间的转换减少,说明其对蓝光和绿光的探索减少。
H:弦图(chord diagrams)显示Red High和Equal条件下的单向转换(unidirectional transitions)。
弦的粗细表示转换频率,HHcy小鼠从蓝光到绿光、蓝光到白光等的转换减少。
I:柱状图展示Red High和Equal条件下的单向转换次数。
更直观地显示HHcy小鼠在颜色臂之间的探索行为减少,尤其是对蓝光相关路径的回避。
图2:HHcy增加视杆与视锥细胞相关基因表达
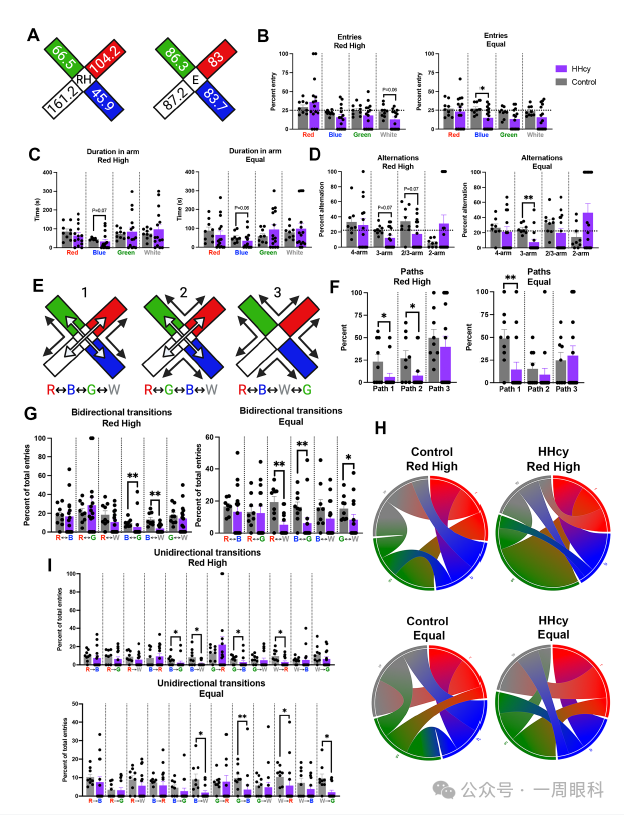
图注翻译与解释:
A:视杆细胞特异性标志物的基因表达变化。
包括Cnga1、Pdc、Pde6g、Rho、Sag等基因,HHcy组中Pde6g显著上调,其余也有上升趋势,提示视杆细胞可能受损或代偿性增生。
B:视锥细胞特异性标志物的基因表达变化。
包括Cngb3、Gnat2、Gngt2、Opn1mw、Opn1sw、Pde6c等基因,HHcy组中Gngt2和Pde6c显著上调,提示视锥细胞也可能出现代偿性反应。
图3:HHcy未显著改变视网膜小胶质细胞或星形胶质细胞数量与体积
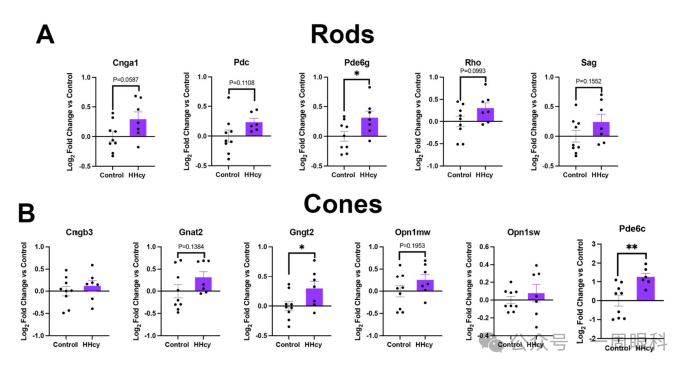
图注翻译与解释:
A:对照组与HHcy组小鼠内层视网膜中IBA-1(小胶质细胞)染色的代表性图像。
显示小胶质细胞的分布与形态,比例尺为100μm。
B:对照组与HHcy组小鼠外层视网膜中IBA-1染色的代表性图像。
C:对小胶质细胞数量、平均体积和总体积的定量分析。
各指标在两组间无显著差异,提示HHcy未引起小胶质细胞明显激活或形态改变。
D:对照组与HHcy组小鼠内层视网膜中GFAP(星形胶质细胞)染色的代表性图像。
E:对照组与HHcy组小鼠外层视网膜中GFAP染色的代表性图像。
F:对星形胶质细胞数量、平均体积和总体积的定量分析。
同样无显著差异,提示HHcy未引起星形胶质细胞明显反应。
图4:HHcy减少血管数量及小胶质细胞与血管的接触
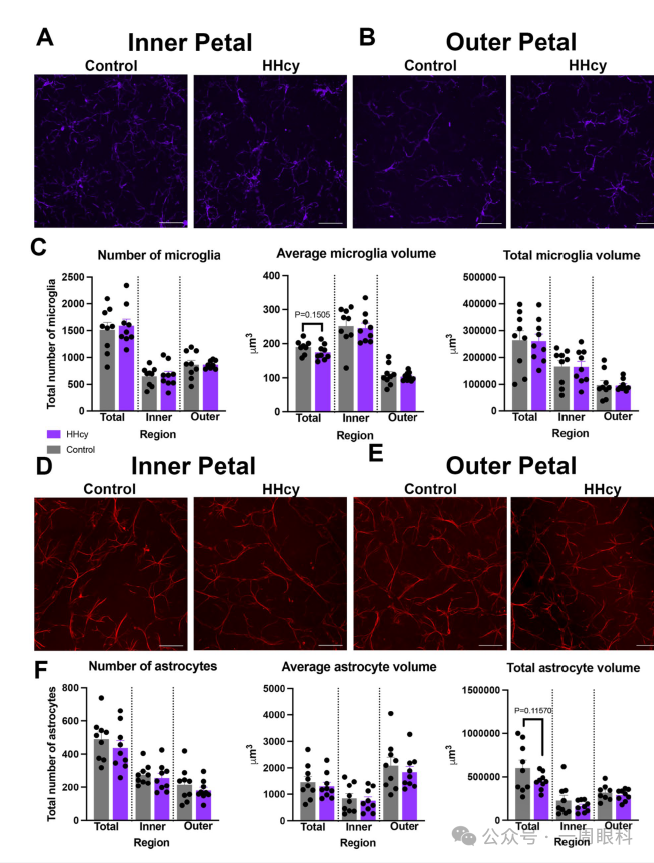
图注翻译与解释:
A、B:对照组与HHcy组小鼠内层与外层视网膜中IBA-1(小胶质细胞)、GFAP(星形胶质细胞)与Ly6c(血管)染色的合并图像。
显示三种结构的相对位置与关系,比例尺为100μm。
C:血管数量的定量分析。
HHcy小鼠血管数量略有减少,尤其在内层视网膜。
D:血管总体积的定量分析。
HHcy组血管总体积显著减少。
E:单个血管平均体积的分析。
无显著差异,说明血管变细但体积不变。
F:血管主轴长度(major axis length)的测量。
内层视网膜中HHcy组血管主轴长度增加,提示血管形态发生改变。
G:与血管接触的小胶质细胞和星形胶质细胞总数量的定量。
H:仅小胶质细胞与血管接触的数量分析。
HHcy组外层视网膜中显著减少。
I:仅星形胶质细胞与血管接触的数量分析。
无显著变化。
J:小胶质细胞与星形胶质细胞共同覆盖血管的总体积分析。
K:仅小胶质细胞覆盖血管的体积分析。
HHcy组略有减少,提示小胶质细胞对血管的支持作用减弱。
L:仅星形胶质细胞覆盖血管的体积分析。
无显著变化。
图5:HHcy下调神经炎症与心血管相关基因表达
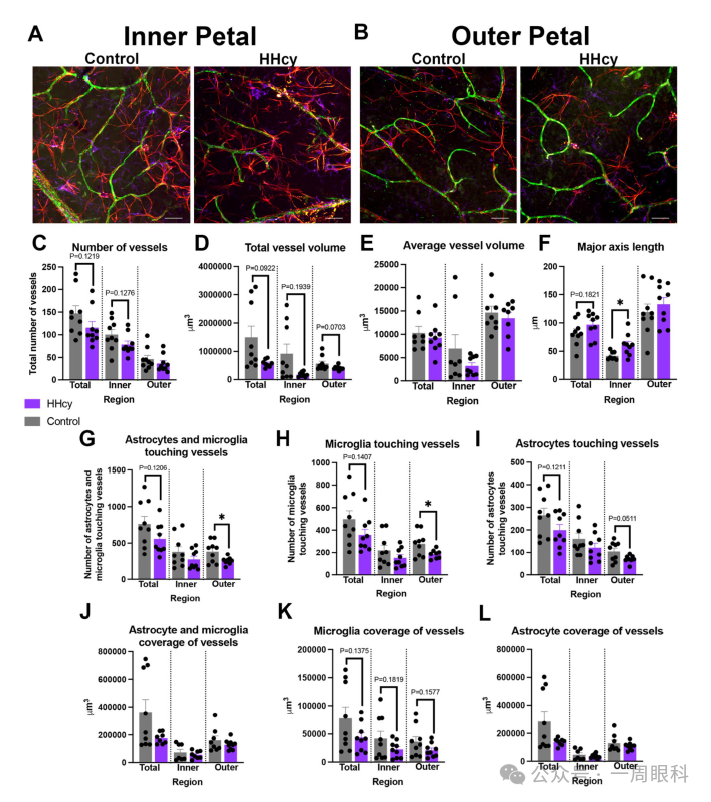
图注翻译与解释:
A:神经炎症与心血管相关基因的火山图(volcano plots)。
横轴为log2 fold change,纵轴为-log10 p值。图中显示HHcy组中多数基因表达下调。
B:STRING数据库构建的蛋白互作网络图。
显示差异表达基因之间的相互作用,涉及Tlr2、Ccl2、Il17a、Nfkbia等炎症信号通路相关基因,提示HHcy可能抑制部分免疫与炎症反应。图自文献,侵权删。
声明:本文仅供医疗卫生专业人士学术交流,不代表本平台观点。该等信息不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议,如果该信息用于资讯以外的目的,本平台及作者不承担相关责任。








